|
°°
µ⁄“ªΩ⁄ ú’˝¿Î◊”
°°
∫¨”–¥¯”–’˝µÁ∫…µƒ»˝º€Ãº‘≠◊”µƒª˘Õ≈£¨ «”–ª˙ªØ—ß∑¥”¶÷–≥£º˚µƒªÓ–‘÷–º‰Ã°£∫Ð∂ý¿Î◊”–Õµƒ∑¥”¶ «Õ®π˝…˙≥…ú’˝¿Î◊”ªÓ–‘÷–º‰ÃÂΩ¯––µƒ£¨Õ¨ ±Ãº’˝¿Î◊”“≤ «—–æøµ√◊Ó‘Á°¢◊ӅӻεƒªÓ–‘÷–º‰Ã£¨∫Ð∂ý—–æø∑¥”¶¿˙≥õƒª˘±æ∏≈ƒÓ∫Õ∑Ω∑®∂º∆ º”⁄ú’˝¿Î◊”µƒ—–æø£¨“Ú¥À£¨”–»À»œŒ™Ãº’˝¿Î◊”µƒ—–æø «¿Ì¬€”–ª˙ªØ—ßµƒª˘¥°°£
“ª£Æú’˝¿Î◊”µƒ…˙≥…
ú’˝¿Î◊”ø…“‘Õ®π˝≤ªÕ¨∑Ω∑®≤˙…˙£¨÷˜“™”–œ¬√Ê»˝÷÷£∫
1£Æ÷––‘ªØ∫œŒÔ“Ï¡—£¨÷±Ω”¿Î◊”ªØ
ªØ∫œŒÔ‘⁄¿ÎΩ‚π˝≥Ã÷–£¨”Îú‘≠◊”¡¨Ω”µƒª˘Õ≈¥¯◊≈“ª∂‘µÁ◊”¿Î»•£¨∑¢…˙π≤º€º¸µƒ“Ï¡—£¨∂¯≤˙…˙ú’˝¿Î◊”£¨’‚ «…˙≥…ú’˝¿Î◊”µƒÕ®≥£Õææ∂°£
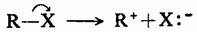
√˜œ‘µƒ µ¿˝»Á£∫

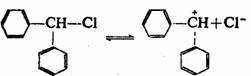
‘⁄’‚—˘µƒπ˝≥Ã÷–£¨º´–‘»Ðº¡µƒ»Ðº¡ªØ◊˜”√ «…˙≥…ú’˝Ãº¿Î◊”µƒ÷ÿ“™Ãıº˛°£∑¥”¶…˙≥…ƒ—»ÐΩ‚µƒ≥¡µÌ“≤ø…”∞œÏ∆Ω∫‚£¨ π∑¥”¶œÚ”“Ω¯––£¨∂¯”–¿˚”⁄ú’˝¿Î◊”µƒ…˙≥…£¨¿˝»ÁAg+ø…“‘∆µΩ¥þªØú’˝¿Î◊”…˙≥…µƒ◊˜”√°£
R-Br + Ag °˙ AgBr°˝ + R+
SbF5◊˜Œ™LewisÀ·£¨”÷ø……˙≥…Œ»∂®µƒSbF6-£¨“≤”–¿˚”⁄ú’˝¿Î◊”µƒ…˙≥…°£
R-F + SbF5
°˙ R+ + SbF6-
‘⁄À·ªÚLewisÀ·µƒ¥þªØœ¬£¨¥º°¢√—°¢ı£¬±“≤ø…“‘¿ÎΩ‚Œ™Ãº’˝¿Î◊”£¨¿˝»Á£∫
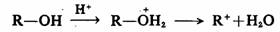
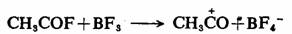
¿˚”√À·–‘Ãÿ«øµƒ≥¨À·…ı÷¡ø…“‘¥”∑«º´–‘ªØ∫œŒÔ»ÁÕÈÃ˛÷–£¨∂·»°∏∫«‚¿Î◊”£¨∂¯…˙≥…ú’˝¿Î◊”°£
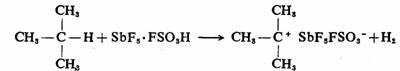
”…”⁄ú’˝¿Î◊”‘⁄≥¨À·»Ð“∫÷–Ãÿ ‚µƒŒ»∂®–‘£¨∫Ð∂ýú’˝¿Î◊”Ω·ππ∫Õ–‘÷ µƒ—–æø «‘⁄≥¨À·÷–Ω¯––µƒ£¨¿˚”√≥¨À·ø…“‘÷∆±∏–Ì∂ý≤ªÕ¨Ãº’˝¿Î◊”µƒŒ»∂®»Ð“∫°£
2£Æ’˝¿Î◊”∂‘÷––‘∑÷◊”º”≥…£¨º‰Ω”¿Î◊”ªØ
÷ ◊”ªÚ¥¯µÁ∫…µƒª˘Õ≈‘⁄≤ª±•∫Õº¸…œµƒº”≥…“≤ø……˙≥…ú’˝¿Î◊”°£

»Áœ©º¸”ά±ªØ«‚µƒº”≥…£¨µ⁄“ª≤Ω…˙≥…ú’˝¿Î◊”°£
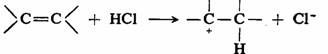
Ù ª˘À·¥þªØµƒ«◊∫Àº”≥…£¨ ◊œ»÷ ◊”ªØ–Œ≥…ú’˝¿Î◊”£¨∏¸”–¿˚”⁄«◊∫À ‘º¡Ω¯π•°£
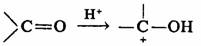
∑ºª∑…œµƒ«◊µÁ»°¥˙∑¥”¶£¨»ÁœıªØ «”…+NO2’˝¿Î◊”Ω¯π•£¨–Œ≥…¶“¬Á∫œŒÔ£¨’‚ «¿Î”ڪصƒÃº’˝¿Î◊”°£

3£Æ”…∆‰À˚’˝¿Î◊”…˙≥…
ú’˝¿Î◊”ø…“‘”…∆‰À˚’˝¿Î◊”◊™±‰µ√µΩ£¨¿˝»Á÷ÿµ™ª˘’˝¿Î◊”æÕ∫лð“◊Õ—µ™∂¯…˙≥…∑ºª˘’˝¿Î◊”°£
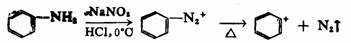
“≤ø…“‘Õ®π˝“ª–©Ωœ“◊ªÒµ√µƒ’˝¿Î◊”∂¯÷∆±∏∏¸Œ»∂®µ´ƒ—”⁄ªÒµ√µƒÃº’˝¿Î◊”£¨¿˝»Á”√»˝±Ωº◊ª˘’˝¿Î◊”ø…“‘∂·»°ª∑∏˝»˝œ©µƒ∏∫«‚¿Î◊”∂¯ªÒµ√ ¿Î◊”°£ ¿Î◊”°£
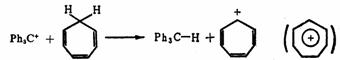
∂˛£Æú’˝¿Î◊”µƒΩ·ππ
ú’˝¿Î◊”¥¯”–’˝µÁ∫…£¨÷––ƒÃº‘≠◊”Œ™»˝º€£¨º€µÁ◊”≤„Ωˆ”–¡˘∏ˆµÁ◊”£¨∆‰ππ–Õ”–¡Ω÷÷ø…ƒÐ£∫“ª÷÷ «÷––ƒÃº‘≠◊”¥¶”⁄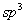 ‘”ªØ◊¥Ã¨À˘–Œ≥…µƒΩ«◊∂–Œππ–Õ£¨“ª÷÷ « ‘”ªØ◊¥Ã¨À˘–Œ≥…µƒΩ«◊∂–Œππ–Õ£¨“ª÷÷ «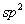 µƒ‘”ªØ◊¥Ã¨À˘–Œ≥…µƒ∆Ω√Êππ–Õ°£≤ª¬€ µƒ‘”ªØ◊¥Ã¨À˘–Œ≥…µƒ∆Ω√Êππ–Õ°£≤ª¬€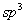 ªπ « ªπ «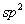 £¨÷––ƒÃº‘≠◊”∂º «“‘»˝∏ˆ‘”ªØπϵ¿£¨”λ˝∏ˆ≥…º¸‘≠◊”ªÚª˘œý¡¨ππ≥…»˝∏ˆ¶“º¸£¨∂º”ýœ¬“ª∏ˆø’πϵ¿°£≤ªÕ¨µƒ ««∞’þµƒø’πϵ¿ « £¨÷––ƒÃº‘≠◊”∂º «“‘»˝∏ˆ‘”ªØπϵ¿£¨”λ˝∏ˆ≥…º¸‘≠◊”ªÚª˘œý¡¨ππ≥…»˝∏ˆ¶“º¸£¨∂º”ýœ¬“ª∏ˆø’πϵ¿°£≤ªÕ¨µƒ ««∞’þµƒø’πϵ¿ «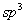 ‘”ªØπϵ¿£¨∂¯∫Û’þø’◊≈µƒ «Œ¥‘”ªØµƒ ‘”ªØπϵ¿£¨∂¯∫Û’þø’◊≈µƒ «Œ¥‘”ªØµƒ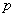 πϵ¿°£ πϵ¿°£
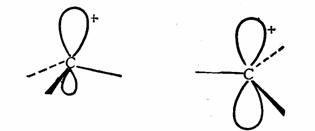
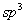 ‘”ªØ ‘”ªØ
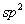 µƒ‘”ªØ µƒ‘”ªØ
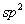 ‘”ªØµƒ∆Ω√Êππ–ձ̜÷¡À∏¸¥ÛµƒŒ»∂®–‘£¨’‚¥”µÁ◊”–ß”¶∫Õø’º‰–ß”¶…œ¿ÌΩ‚∂º «±»Ωœ∫œ¿Ìµƒ°£‘⁄∆Ω√Êππ–Õ÷–£¨¶“º¸µƒº¸Ω«Œ™120°££¨”Î109.5°£±»Ωœ¶“º¸µÁ◊”∂‘÷ƺ‰µƒB-’≈¡¶Ωœ–°°£Õ¨ ± ‘”ªØµƒ∆Ω√Êππ–ձ̜÷¡À∏¸¥ÛµƒŒ»∂®–‘£¨’‚¥”µÁ◊”–ß”¶∫Õø’º‰–ß”¶…œ¿ÌΩ‚∂º «±»Ωœ∫œ¿Ìµƒ°£‘⁄∆Ω√Êππ–Õ÷–£¨¶“º¸µƒº¸Ω«Œ™120°££¨”Î109.5°£±»Ωœ¶“º¸µÁ◊”∂‘÷ƺ‰µƒB-’≈¡¶Ωœ–°°£Õ¨ ±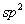 πϵ¿”Î πϵ¿”Î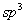 πϵ¿±»«∞’þ”–Ωœ∂ýµƒS≥…∑÷£¨¶“º¸µƒµÁ◊”∂‘∏¸øøΩ¸Ãº‘≠◊”∫À£¨“≤∏¸Œ™Œ»∂®°£¡ÌÕ‚£¨ø’µƒ πϵ¿±»«∞’þ”–Ωœ∂ýµƒS≥…∑÷£¨¶“º¸µƒµÁ◊”∂‘∏¸øøΩ¸Ãº‘≠◊”∫À£¨“≤∏¸Œ™Œ»∂®°£¡ÌÕ‚£¨ø’µƒ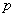 πϵ¿…Ï’π”⁄∆Ω√Ê¡Ω≤ý£¨±„”⁄»Ðº¡ªØ°£ πϵ¿…Ï’π”⁄∆Ω√Ê¡Ω≤ý£¨±„”⁄»Ðº¡ªØ°£
°°
π≤ 2 “≥ 1
2 |