7-4-2金属键的能带理论
洛伦兹(Lorentz)首先提出金属的电子海理论(图7-31),认为金属是由阳离子排列在自由电子的海洋中组成的。电子海理论不能较好地解释诸如高熔点,高的原子化热和硬度等问题。按电子海理论,金属键强度应随价电子数增加而增大,高熔点的峰值不应出现在6族(6B)。基于分子轨道理论的能带理论能较好地解释这些问题。
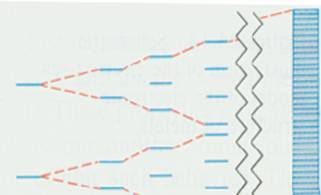
一片金属可看作一个无限的分子,在其中所有原子都按密堆积型式排列。如果大量的钠原子聚集在一起,3s价轨道的相互作用将产生一组非常密集的分子轨道,如下图所示。因为每个分子轨道都离域到金属中的全部原子,金属钠的能态较适合于参照分子轨道来了解。能态的完整谱带称为能带。

在一个能带中,能态的分布并不均匀,能带的结构可较好地用能量E对态密度函数N(E)作图表示,如图7-32所示。态密度函数表达出处在能量为E和E+δE间能态的数目。
在每个能带中,能态的数目等于由全部原子提供的轨道的总数。对1mol的金属,一个s能带将由N0个态组成,而一个p能带则由3N0个态组成,这里N0表示Avogadro数。如果s和p轨道能级差大,这些能带保持分立状态。但是如果s和p轨道能级差小,能带会互相重叠并发生混杂。
固体的电子性质和能带结构密切地相关。根据能带的分布和电子填充情况,能带有不同的性质和名称:充满电子的能带叫满带,能级最高的满带叫价带;完全没有电子的能带叫空带,能级最低的空带叫导带;各能带间不能填充电子的区域叫带隙,又称为禁带。若一种材料只有全满和全空的能带,它不能改变电子的运动状态,故不能导电。含有部分填充电子的能带的材料才能导电,才是真正导电的能带。如果满带和空带重叠,它们合在一起形成一个未填满的能带。金属的能带特征就是有未填满电子的能带。绝缘体的能带特征是只有满带和空带,而且能量最高的满带(价带)和能量最低的空带(导带)之间的带隙很宽,Eg≥5eV;在一般的电场条件下,难把价带上的电子激发到导带而导电。半导体的能带结构特征也是只有满带和空带。但价带和导带之间的带隙较窄,Eg≤3eV。在0K时,电子从最低能级逐一往上填充,电子占据的最高能级称为Fermi能级EF。根据上述情况,固体的能带结构有四种基本的类型,示于图7-33中。
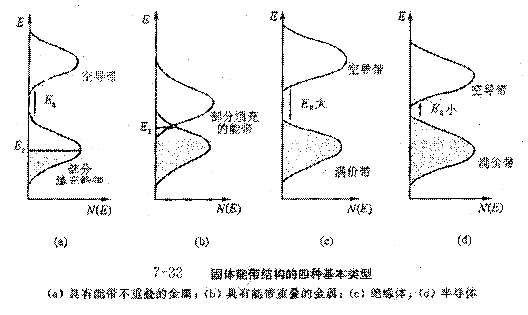
金属的价电子按分子轨道理论的基本原理填充在这些能带中。在金属钠和金属铜中,由价层s轨道叠加形成的半充满s能带是部分填充的能带,如图7-33(a)。碱土金属和第12族金属(Zn,Cd,Hg)有着全充满的s能带,但由于s-p混杂,由满带和空带互相重叠而形成部分填充的能带,如图7-33(b)。所以这些元素是很好的金属导体。绝缘体的价带和导带由较大的带隙隔开,如图7-33(c)所示。金刚石中的C原子,由于s轨道和p轨道杂化成四面体的杂化轨道,在晶体中原子间的距离下,分裂成成键轨道和反键轨道,成键轨道组成价带,反键轨道组成导带,带隙宽度Eg=5.47eV,所以金刚石是绝缘体。Si和Ge的Eg较小,形成半导体,如图7-33(d)。
所形成的能带不能被参加成键的电子充满,产生了金属的特性:
(i)电和热的优良导体。由于能级差小,电子容易跃迁,自由电子的运动产生良好的导电,导热性;
(ii)高密度。每个金属原子将在空间允许的条件下,与尽可能多数目原子形成金属键。金属结构总是按最紧密的方式堆积起来。
好的延展性。金属离子能够移动而不需破坏化合键。金属变形同时伴随着电子的重新分布。
能带理论对熔点等性质的变化趋势的解释是:在过渡金属中,如果价层s、p、d轨道叠加,每个原子所产生的能带(9个小能级),可以容纳2+6+10=18个电子,能带中的低能级部分容纳9个价电子,此时达到最大键级和键强。高能级部分可容纳另外9个价电子。如果仅s和d轨道叠加,每个原子的最大键级为6个电子。所以,高的熔点,原子化热,硬度和密度出现在6~8族(6B~8B, 6~9个价电子)。