|
��
�����ϰ��
4-1
�ӻ�ѧʽ���������Ǹ߶Ȳ����͵Ļ����Ϊʲô���������ӳɷ�Ӧ��
��
���Ħе��������γɱպϵĹ�����ϵ��ʹ��ϵ������2�µ������ܣ�ʹ���ر��ȶ�����������ӳɷ�Ӧ�����ƻ������ȶ��Ĺ�����ϵ��
4-2
Ϊʲô���ڴ��⻯ʱ��һ�������ɻ����飿
��
����ϩ�ͻ�����ϩ���ȱ����á������⻯����-208��2kJ/mol������ϩ��-119��6kJ/mol��������ϩ��-231��4kJ/mol������ֻ��һ����������ɻ�����ϩ����ϵ����������23��2kJ/mol��
��-3
���л�״�������Щ�Ƿ����ӻ�������á�O��Ȧ���ӻ�����������ԭ�Ӳ����γɷ���е�����ϵ��δ���õ��Ӷԡ�
��
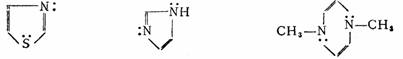
��a��
��b��
��c��
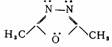
(d)
�⡡
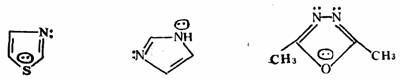
��a��
��b��
��d��
4-4
Ԥ�����е�����ϩ����a��C9H10
��b��C9H9+
��c��C9H9-�����з����ԣ�
��
��a������ʽΪC9H10�ĵ�����ϩ������������Ͷȣ��ǻ�����ϩ���а˸��е����ҹ���û�бպϣ�û�з����ԡ���b��C9H9+���а˸��е��Ӳ������ݿ˶�����û�з����ԡ���c��C9H9-�ǻ�����ϩ�����ӣ�����10���е��ӵĻ�״�պϵĹ�����ϵ�������ݿ˶������з����ԡ�
4-5
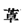 ͪA��һ���ȶ��Ļ�����ܷ�����ȡ����Ӧ���������ϩͪ�·dz����ã����Է��Ķ��ۡ�Ϊʲô�� ͪA��һ���ȶ��Ļ�����ܷ�����ȡ����Ӧ���������ϩͪ�·dz����ã����Է��Ķ��ۡ�Ϊʲô��
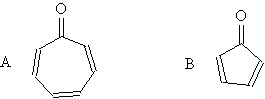
��
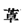 ͪA��ż�������ӻ�����һ������6���е��ӵķ����Խṹ�� ͪA��ż�������ӻ�����һ������6���е��ӵķ����Խṹ��
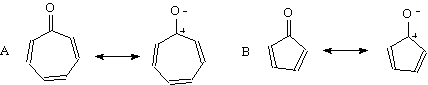
�����ϩͪ�ġ�ż�������ӻ��塱��һ������4���е��ӵķ������Խṹ,��˷dz����á�
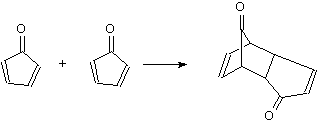
4-6
����������������������?
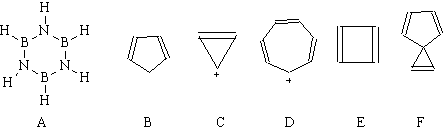
�⡡���з����Ե��У����á��ĺͣơ������ü��ĵ����������������ݿ˶�����,�ƵĽṹ����ʽ��ʾ��Ϊ���ʣ�����ʽ�������Կ����Ƶķ�����������

��
4-7
�����������۲쵽������������������Ժͼ��Զ�������ǿ������������DZ�������स����ļ
������������Ĺ������빲��������ȶ�����������������ȵļ���ʽ������ɻ�ɷֲ���������ԭ���϶��õ���ɢ��������û�����������
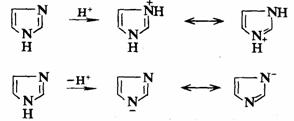
��������व�ԭ���ϵ�δ���õ��ӶԴ���SP2�ӻ������������व�ԭ���ϵ�δ���õ��ӶԴ���SP3�ӻ�����������ӻ�ЧӦ����वĵ�ԭ�ӽ�������वĵ�ԭ���ѽ�����ӡ�
4-8
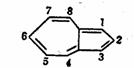
 �����������֣�azulene��,
����ɫ���壬�ֳ��������۵�99�档������һ����Ԫ����һ����Ԫ�����϶��ɵġ�ż����Ϊ1��08D����X-���߷��͵������䷨�ⶨ�����ļ���������ȣ����ɷ�����ȡ����Ӧ����ν�����Щ���� �����������֣�azulene��,
����ɫ���壬�ֳ��������۵�99�档������һ����Ԫ����һ����Ԫ�����϶��ɵġ�ż����Ϊ1��08D����X-���߷��͵������䷨�ⶨ�����ļ���������ȣ����ɷ�����ȡ����Ӧ����ν�����Щ����
��
 ����һ����Ԫ�Ļ����ϩ����Ԫ���Ļ�����ϩ���϶��ɣ��������Եļ��ԣ�������Ԫ���Ļ����ϩ���Ǹ��ģ���Ԫ���Ļ�����ϩ�������ģ��ɱ�ʾ���£� ����һ����Ԫ�Ļ����ϩ����Ԫ���Ļ�����ϩ���϶��ɣ��������Եļ��ԣ�������Ԫ���Ļ����ϩ���Ǹ��ģ���Ԫ���Ļ�����ϩ�������ģ��ɱ�ʾ���£�
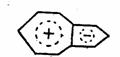
ÿ�������з����ԣ����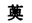 Ҳ���з����ԣ��������ij����DZ�����֮һ�������ϩ���Ǹ����ӵģ���ȡ����Ӧ�����ڻ����ϩ����1λ��3λ�ϣ� Ҳ���з����ԣ��������ij����DZ�����֮һ�������ϩ���Ǹ����ӵģ���ȡ����Ӧ�����ڻ����ϩ����1λ��3λ�ϣ�
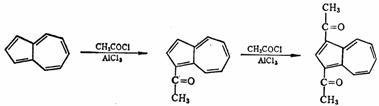
4-9
��10����ϩ�����ԣ���1��6-�Ǽס�10����ϩ�ѱ�֤�����з����ԣ�Ϊʲô��
��
[10]��ϩ���е���������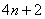 �����м�������ԭ�ӱ˴˸��ţ�ʹ���������Ӳ�������һ��ƽ���ϣ���Ҳû�з����ԡ�����1��6-λ�����Ǽ�����������������������ԭ�ӵ�����ţ�ʹ���ӻָ���ƽ��ṹ�����1��6-�Ǽס�10����ϩ�з����ԡ����Ǹ��Ƚ��ȶ��Ļ����NMR������Ħ���6��9��7��3�� �����м�������ԭ�ӱ˴˸��ţ�ʹ���������Ӳ�������һ��ƽ���ϣ���Ҳû�з����ԡ�����1��6-λ�����Ǽ�����������������������ԭ�ӵ�����ţ�ʹ���ӻָ���ƽ��ṹ�����1��6-�Ǽס�10����ϩ�з����ԡ����Ǹ��Ƚ��ȶ��Ļ����NMR������Ħ���6��9��7��3��
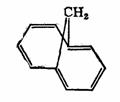
1��6-�Ǽס�10����ϩ
��һҳ
��һ��
|