|
第五节 苯炔
苯炔(benzyne)或叫去氢苯(dehydrobenzene),是苯环亲核取代反应中的活性中间体。苯炔存在的证据,使芳香族亲核取代反应中的许多过去难以解释的现象得到了解决。
一.苯炔的存在及其结构
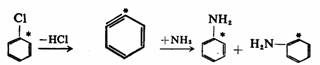
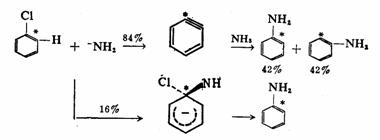
芳烃环上的反应一般是亲电取代反应,芳环上的亲核取代反应是比较困难的,通常要邻位或对位具有强的吸电基时才有可能。在强烈的条件下,如芳卤化物在氨基纳存在下加热,则氨解而转变为芳胺,而且存在一些异常的现象,但其反应历程并非一般亲核取代。例如:
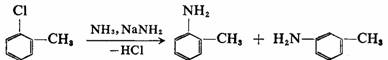
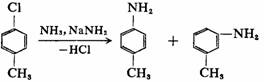
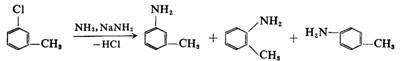
邻氯甲苯氨解得到邻甲苯胺和间甲苯胺,对氯甲苯氨解得到的是对甲苯胺和间甲苯胺,而间氯甲苯氨解则得到邻、间、对三种甲苯胺的混合物。这些实验事实提供了反应是按先消除而后加成历程进行的依据,而且提出了生成活性中间体苯炔的可能。
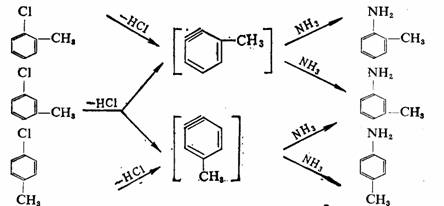
利用C14示踪原子的方法也同样可以提供氯苯的氨解是按生成苯炔的历程,通过消除而后加成进行的。
苯炔的存在还可以通过活性中间体捕集(trapping of
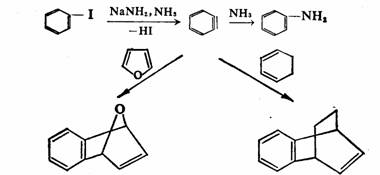
intermediates)的方法得到证实,这对苯炔的生成和存在也提供了有力的证据。例如在碘苯与氨基钠的反应中,加入呋喃或环戊二烯等活泼的双烯体,则可改变苯炔生成后与氨继续反应的正常途径,而与捕集分子生成环加成产物,证明碘苯的氨解不是简单的亲核取代反应,而是消除后再加成的苯炔历程,苯炔中间体确是存在的。
从前面讨论的实验结果看,苯炔是对称的,相当于从苯的相邻两个碳原子上各去掉一个氢原子,形成一个由叁键相连的化合物,其结构式可表示如下:
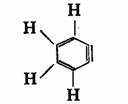
实际上,苯炔中的叁键碳原子仍为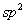 杂化状态,叁键的形成基本上不影响苯环中离域的π体系,苯环的稳定性保持不变,而新的“π键”是由两个 杂化状态,叁键的形成基本上不影响苯环中离域的π体系,苯环的稳定性保持不变,而新的“π键”是由两个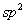 杂化轨道,在环平面内,侧面交盖而形成很弱的键,因此非常活泼,很不稳定。 杂化轨道,在环平面内,侧面交盖而形成很弱的键,因此非常活泼,很不稳定。
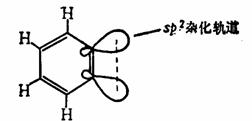
这样的结构是与苯炔高度的化学活性一致的,也是经物理方法所证实的。
二.苯炔的生成
苯炔的生成主要从苯环中相邻两个碳原子上,一个去掉电负性基团,一个除去电正性基团而形成的,可用通式表示如下:
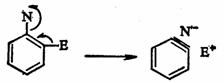
随着反应物和反应条件的不同,苯炔产生的方法主要有以下几种。
1.芳卤化物脱卤化氢
芳香族卤化物与强碱作用,通过β-消除反应而生成芳炔。反应首先是由夺取苯环上的氢(质子)开始的,以烷基或芳基锂在乙醚中,在-30℃进行反应,常常可以得到很好的产率。
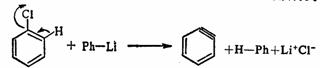
不同的卤原子,生成苯炔的难易程度也不相同,一般氟化物较容易生成苯炔,因为氟的电负性大,使邻位碳原子上的氢酸性增强,更有利于氢作为质子离去。而氟虽然不是好的离去基团,但它处于非控制反应速度的快步骤之中,消除质子的一步是控制反应速度的步骤。
同时,卤原子的直接取代反应也是与生成苯炔的β-消除反应相互竞争而发生,因此,在氯苯的氨解反应中,除了β-消除反应生成苯炔外,实际上还存在直接取代反应的竞争。
共 2 页 1
2
|