| 第四章 紫外-可见吸收光谱法 |
不同物质具有不同的分子结构,对不同波长的光会产生选择性吸收,因而具有不同的吸收光谱。无机化合物和有机化合物吸收光谱的产生在本质上是相同的,都是外层电子跃迁的结果,但二者在电子跃迁类型上有一定的区别。
一、紫外可见光谱与分子结构的关系
(一) 紫外可见光谱的形成
分子中的电子总是处在某一运动状态中,每一种状态都具有一定的能量,属于一定能级。电子由于受到光、热、电等的激发,从一个能级转移到另一个能级,称为跃迁。由于分子内部运动所牵涉到的能级变化比较复杂,分子吸收光谱也就比较复杂。在分子内部除了电子运动状态外,还有核间的相对运动,即核的振动和分子围绕着重心的转动。而按量子力学计算,振动能和转动能是不连续的,具有离子化的性质。分子的总能量是其键能(电子能)、振动能和转动能的总和,当分子从辐射的电磁波吸收能量之后,分子会从低能级跃迁到较高的能级,它的能量变化ΔE为其振动能变化ΔEv、转动能变化ΔEr以及电子运动能量变化ΔEe的总和,即ΔE=ΔEv+ΔEr+ΔEe (4-1)
式(4-1)中ΔEe最大,一般在1~20eV之间
吸收频率决定于分子的能级差,其计算式为:ΔE=hv或ΔE=hc/λ,式中ΔE为分于跃迁前后能级差,v、λ分别为所吸收的电磁波的频率及波长, C为光速,h为普朗克常数。
现假设ΔEe为5eV,其相应波长为
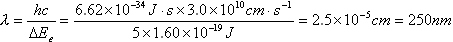
因此,由于分子内部电子能级的跃迁而产生的光谱位于紫外区或可见区内。
分子振动能级间隔ΔEv大约比ΔEe小10倍,一般在0.05-1eV之间。如果ΔEv为0.1eV,即为5eV的电子能级间隔的2%,则在发生电子能级跃迁的同时,必然要发生振动能级之间的跃迁,得到的是一系列的谱线,它们相互波长的间隔是250nm×2%=5nm,而不是250nm单一的谱线。
分子转动能级间隔ΔEr大约比ΔEv小10倍或100倍,一般小于0.05eV。现假设ΔEr为0.005eV ,则为5eV是电子能级间隔的0.1%。当发生电子能级和振动能级之间的跃迁时,必然要发生转动能级之间的跃迁。由于得到的谱线彼此间的波长间隔只有250nm×0.1%=0.25nm,如此小的间隔使它们连在一起,呈现带状,称为带状光谱。
图4-2是电磁波与分子能级相互作用示意图。
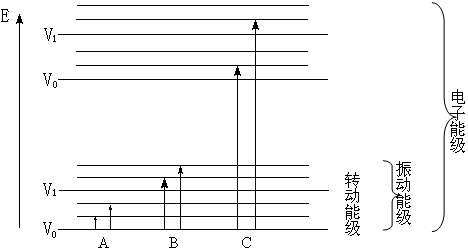 |
| 图4-2 电磁波吸收与分子能级变化 A:转动能级跃迁(远红外区) B:转动/振动能级跃迁(近红外区) C:转动/振动/电子能级跃迁(可见,紫外区) |
| 物质对不同波长的光具有不同的吸收能力,物质也只能选择性地吸收那些能量相当于该分子振动能变化△Eν、转动能变化△Er以及电子运动能量变化△Ee总和的辐射。由于各种分子内部结构不同,分子的能级也千差万别,各种能级之间的间隔也互不相同,这样就决定了它们对不同波长的光线的选择性吸收。如果改变通过某一吸收物质的入射光的波长,并记录该物质在每一波长处的吸光度(A),然后以波长为横坐标,以吸光度为纵坐标作图,这样的谱图称为该物质的吸收光谱或吸收曲线。某物质的吸收光谱反映了它在不同的光谱区域内吸收能力的分布情况,可以从波形,波峰的强度、位置及数目看出来,为研究物质的内部结构提供重要的信息。 (二)电子跃迁类型 有机化合物分子结构中,有成键的σ电子和π电子,不成键的n电子(往往是p电子)。单键是由σ电子组成的,又称σ单键。双键是由σ和π键组成。此外还有未成键的σ*反键和π*反键轨道。各种分子轨道能量高低的顺序为:σ<π<n<π*<σ* 在基态分子中,成键电子占据成键轨道,未成键的孤对电子占据非键轨道。分子吸收紫外或可见辐射后,电子由基态的成键轨道或非键轨道跃迁至激发态的反键轨道。经常遇到的跃迁有σ  σ*、n σ*、n σ*、n σ*、n π*和π π*和π π*四种类型,如图4-3所示。 π*四种类型,如图4-3所示。
|
| 下一页 |