|
第二节 亲核加成反应
醛、酮分子中含有典型的羰基,羧酸及其衍生物中含有广义的羰基。在它们的多数反应中关键的一步是羰基与亲核试剂起加成反应,生成具有四面体结构的中间产物:
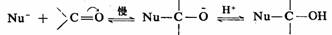
由醛、酮生成的中间产物一般是从溶剂中接授质子变成加成产物,这是简单加成历程,或进而发生β―消除,是复杂加成历程。而由羧酸及衍生物生成的中间产物一般是
离去基团L离去,恢复原来的羰基,生成取代物。两类化合物的产物虽然不同,但历程相似,反应物结构对反应活性的影响也有相似之处,烃基(R)供电子能力越强,空阻越大,反应活性越低。烃基上有吸电子基团则增强反应活性。不同之处是后者的反应活性还与离去基团L-的稳定性及L与羰基之间的电子效应有关。L-的稳定性越大,反应活性越强,―I效应越大、+C效应越小,则反应活泼越强。不同羰基化合物的活性按以下顺序降低:
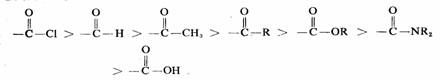
羰基化合物的特征反应是亲核加成反应,这是羰基极化的必然结果。在羰基中,由于极化,羰基碳带部分正电荷,羰基氧带部分负电荷。氧的电负性较大,有较强容纳负电荷的能力,羰基氧是比较稳定的。因此羰基碳是决定羰基反应性能的中心,亲核试剂进攻羰基碳的反应是羰基化合物的特征反应。羰基化合物的亲核加成反应常常是被酸催化。酸催化在于羰基氧原子的质子化,使羰基碳电正性更增加,更有利于亲核试剂的进攻。
一.亲核加成反应历程
1.醛、酮羰基的简单加成反应历程
醛、酮与HCN、NaHSO3、醇以及RMgX等的反应是简单的亲核加成反应。对于同一个羰基化合物,亲核试剂的亲核性增加,平衡常数增大。亲核试剂的亲核性是碳>氮>氧。碳亲核试剂如RMgX、威狄希试剂等对醛、酮的加成效率很高,反应实际上是不可逆的。氮亲核试剂的活性远不如碳亲核试剂,氧亲核试剂的活性更低。
醛、酮与醇反应生成生成半缩醛、酮,平衡常数小于1。反应通常被酸
催化。
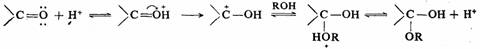
半缩醛(酮)转化为缩醛(酮)则需要干燥的HCl催化:
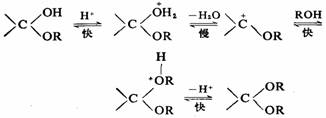
缩醛(酮)用稀酸处理水解为原来的醛酮,在有机合成上可用缩醛(酮)保护羰基。
醛、酮与HCN的亲核加成反应需在微量碱存在下进行,-CN是强碱,又有较大的可极化性,是一个强的亲核试剂。反应历程如下:
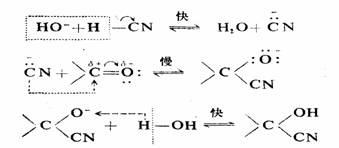
反应也是可逆的。反应生成的氰醇是重要的合成中间体。
2.醛、酮羰基的复杂加成反应历程
醛、酮和氨及其衍生物的加成反应,为加成―消除历程。先发生加成反应,继而发生β―消除,生成含有C=N化合物。
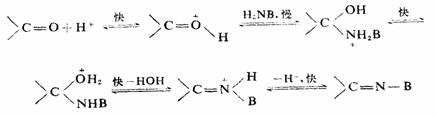
式中的B可为H、R、Ar、OH、NH2、NHR、NHAr、NHCONH2。这些反应为适量H+所催化。但〔H+〕过大时反会降低试剂NHB的浓度,结果导致反应速度下降。
3.羧酸衍生物中羰基的亲核加成反应
羧酸及其衍生物的反应大多数是通过加成―消除历程进行的:
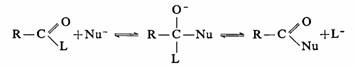
L: -OH
、-X、-OCOR、-OR、-NH2
Nu-:
OH-、H2O、NH3、ROH等
此类反应中研究得最充分的是酯的水解反应。大多数酯在碱性溶液中的水解反应属于酰氧断裂的双分子反应,即BAC2历程(B表示碱性水解,
AC表示酰氧断裂,2表示速度决定步骤为双分子反应):
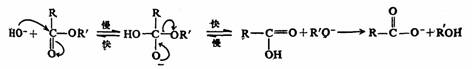
反应最后一步是不可逆的,因为生成的RCOO-是比RO-是弱得多的碱,不可能攫取醇中的质子,从而使整个反应变为不可逆。
多数的酯在酸性溶液中的水解反应也属于酰氧断裂的双分子反应,简称AAC2历程(A表示酸性水解,AC表示酰氧断裂,2表示速度决定步骤为双分子反应)。其步骤与碱性水解相似,但反应是可逆的。
本节共 3 页 1
2
3 |