|
问题和习题
8-1
解释为什么炔烃的亲电加成反应没有烯烃的反应活性高?
解
炔烃叁键的碳原子是SP杂化,烯烃双键碳原子是SP2杂化,SP杂化比SP2杂化的轨道半径短,电负性大,叁键中的电子被束缚得比双键中的牢,亲电试剂夺取叁键中的电子较困难,所以,炔烃的亲电加成反应没有烯烃活泼。如在同一化合物中同时有碳碳双键和叁键,亲电试剂首先与碳碳双键加成:

90%
正由于叁键与电子的结合力较强,炔烃能发生亲核加成反应。例如,炔烃可与强亲核试剂如RO-(在醇中)进行反应,生成烯基醚。
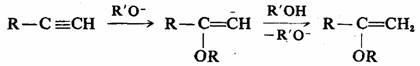
如果使用弱的亲核试剂则需要加入催化剂,常用的催化剂是Hg2+离子,因为它能与叁键配位,从叁键吸引电子,有利于弱亲核试剂的进攻。例如炔烃的水合反应:
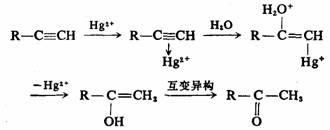
若炔烃是乙炔,水合产物是乙醛,这就是著名的库切洛夫(Кучеров)反应。
8-2
溴与一些烯烃的加成反应速率有以下结果:
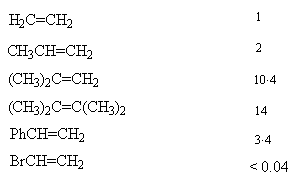
烯烃
相对速率
怎样解释这些数据
?
解
从这些数据可以看出,双键碳原子上烷基数目增多,反应速率加快,因此反应速率与空间效应关系不大,与电子效应有关,烷基有给电子的诱导效应和超共轭效应,使双键上电子云密度增大,烷基取代越多,反应速率越快。当双键与苯环相连时,苯环通过共轭体系起了推电子效应,因此加成速率比乙烯快,当双键与溴相连时,溴的拉电子诱导效应超过给电子效应,总的结果起了吸电子作用,因此加成速率大大降低。
8-3
烯烃与溴在不同介质中进行反应得如下结果:
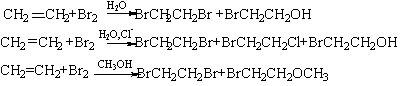
上述三个反应速率相同。这个结果说明了烯烃与溴的反应过程经历了什么样的反应历程?
解
反应是分两步进行的。每个反应中均有BrCH2CH2Br
产生,说明反应的第一步均为Br+与CH2=CH2的加成,又由于三个反应速率相同,说明这
步是决定反应速率的一步;第二步是反应体系中各种负离子进行加成,是快反应的一步。
8-4
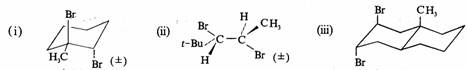
写出下列化合物与溴的加成产物。
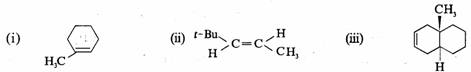
解
8-5
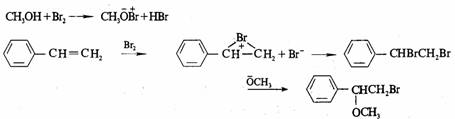
苯乙烯在甲醇溶液中溴化,生成1-苯基-1,2-二溴乙烷和1-苯基-1-甲氧基-2-溴乙烷,试用反应历程解释。
解
8-6
氯化氢与3-甲基环戊烯反应生成1-甲基-2-氯环戊烷和1-甲基-1-氯环戊烷的混合物,写出反应历程及中间体,并加以解释。
解
反应有重排产物,说明加成反应是按碳正离子AdE2历程进行的:
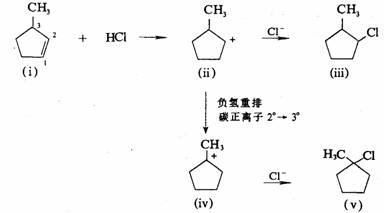
由于甲基的给电子效应,使(ⅰ)的C-1的电子云密度增加,H+与(ⅰ)反应生成(ⅱ),(ⅱ)与Cl-结合生成(ⅲ)1-甲基-2-氯环戊烷。因(ⅳ)稳定,(ⅱ)重排成(ⅳ),(ⅳ)再与与Cl-结合生成(ⅴ)1-甲基-1-氯环戊烷。
共 3 页 1
2
3 |