|
明确了上述概念,就可以按下面的几条规则来书写结构式:
(1)共用电子数和未共用电子数的总和必须等于构成分子的中性原子的电子数总和。
(2)每个构成原子价层占有度必须符合原子价层占有度的要求。
(3)在上述的前提下,使共用电子对,即共价键尽可能多,而末共用电子对尽可能少。
(4)如果是离子,则在原于(团)固有的电于数总和再加上(负离子)或减去(正离子)电荷数。
(5)结构式中每个构成原子的形式电荷,可按形式电荷的计算公式计算。
H2SO4
:价电子总数为32,可能的结构式为:
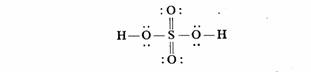
各原子的形式电荷为0。
CH3―NO2
:价电子总数为24,可能的结构式为:
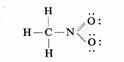
其中N的形式电荷为+1,而其中一个O原子的形式电荷为-1,结构式为:
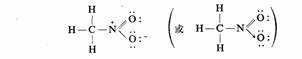
共 3 页
1
2
3
下一节 |