|
四.影响亲核取代反应活性的因素
饱和碳原子上的亲核取代反应可按两种不同的历程进行。但对一种具体反应物来说,在一定条件下,与亲核试剂作用时,究竟主要按什么历程进行?反应活性如何?这与R―L的结构(R和L的结构)、Nu:的性质和溶剂的性质等都有密切关系。有机理论的最近进展已深入到定量地衡量这些因素,这里只简单地说明这些因素是如何影响典型的亲核取代反应的。
1.烃基的结构和空间效应
从烃基的电子效应看,当烃基为烷基时,中心碳原子上取代基越多,供电能力增强,使碳正离子越稳定,对SN1历程越有利,而对SN2历程越不利。当中心碳原子上联有碳碳双键及芳香取代基时,它们解离成碳正离子(按SN1历程)或与Nu:形成过渡态(按SN2历程)由于共轭的原因,都比较稳定。因此,这些基团的存在,不论是对SN1历程或SN2历程都是有利的。虽然不同烃基的电子效应对SN1、SN2历程都有影响。但是在SN2的过渡态里,中心碳原子上只有相当小的电荷,所以烃基的电
子效应对SN2历程的影响一般不及SN1历程显著。
烃基的空间效应对SN1和SN2历程都有一定的影响,一般说,烃基的空间效应对SN2历程的影响远较SN1历程为显著。当中心碳原子上连有叔丁基时对SN2历程的空间影响尤为显著。桥环化合物桥头碳原子的取代反应,无论是SN1还是SN2历程都是很困难的。
2.亲核试剂的性质
取代反应按SN1历程进行时,反应速度只取决于R―L的离解,而与Nu:无关,因此试剂的亲核性能的改变,对反应速度不发生明显影响。
取代反应按SN2历程进行时,亲核试剂参与了过渡态的形成,其亲核性能的改变对反应速度将产生一定影响。一般说来,试剂的亲核能力越强,形成过渡态所需的活化能越低,SN2反应的趋向越大。
关于亲核试剂的强度是一个复杂的问题,对于其强度的精确描述是困难的,因为这不仅决定于亲核试剂的本身性质,而且决定于所选用的实验条件、反应物的结构、溶剂、离去基团等对试剂的亲核性都有影响,所以只能得到亲核性的相对强度,不可能列出亲核性强度的绝对顺序。同一试剂在不同的反应中则可能显示不同的亲核性。
一般认为试剂亲核性的强弱,决定于它所带电荷的性质、碱性强弱、可极化性大小和有效体积的大小。
一个带负电荷的亲核试剂要比相应呈中性的试剂更为活泼。试剂的亲核性能大致与其碱性强弱次序相对应。这里应该注意亲核性与碱性是既有区别又有联系的两个不同概念。亲核性代表试剂与碳原子的结合能力,碱性代表试剂与氢原子结合的能力,它们的强弱次序并不完全一致。对具有相同进攻原子的亲核试剂,碱性愈强者,其亲核活性也愈强。
C2H5O->HO->C6H5O->CH3COO-
对周期表中同周期元素组成的负离子的亲核试剂,也和它们的碱性强弱次序大致呈对应关系:
R3C->R2N->RO->F-
但对同一族元素来说,情况比较复杂。以第七族为例,在非质子溶剂(如二甲亚砜、N,N-二甲基甲酰胺等)中,卤离子的碱性和亲核能力都随进攻原子序数的增加而减弱,F->CI->Br->I-,显示出对应关系。但
在醇等质子溶剂中,卤离子的亲核能力却随着下列次序降低I->Br->CI->F-,这是由于卤离子与质子溶剂之间存在着氢键,可以使卤离子的亲核性能减弱,而F-与其他卤离子相比,与质子溶剂之间形成的氢键最强,因此也就相对地表现为一个弱的亲核试剂。
亲核试剂的可极化性不同,对亲核能力也有一定影响
。亲核试剂的可极化性是它的电子云在外界电场影响下变形难易的量度。亲核试剂的可极化性越大,它进攻碳原子时,其外层电子越容易变形而伸向中心碳原子,从而降低了形成过
渡态时所需的活化能。因此试剂的可极化性越大,其亲核性也越强。对同族元素来说离子可极化性次序如下:
I->Br->Cl->F-
亲核试剂也往往呈现出一定的空间效应。例如,烷氧基负离子的碱性强弱次序为(CH3)3CO->C2H5O->CH3O-。但它们在SN2反应中亲核能力的强弱次序则与此相反。这是由于第三丁氧基有效体积较大,进攻碳原子受阻也较大,不易进行亲核取代反应。而较易作为一个碱去进攻质子。根据这个道理,我们很容易理解线形结构的亲核试剂如CN-等在SN2反应中应具有特殊的活泼性。下表为一些代表性的亲核试剂和它们的相对活性:
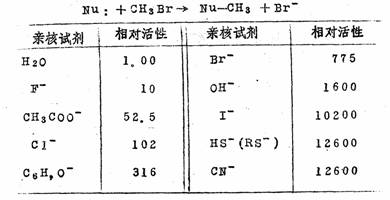
3.离去基团的性质
亲核取代反应无论按那种历程进行,离去基团总是带着电子对离开中心碳原子,这与亲核试剂总是带着电子对向中心碳原子进攻的情况正好相反。所以离去基团性质的改变对SN1和SN2反应产生的影响是相似的。离去基团离去的难易与它的碱性强弱、可极化性的大小、以及溶剂的性质等都有关系。离去基团的碱性越弱,越容易离开中心碳原子,即反应物越容易被取代。例如,含氧离去基团活性次序随着碱性的增强而减弱:
RSO3->RCOO->C6H5O-
碱性很强的基团如R3C-、R2N-、RO-、HO-等根本不能作为离去基团而进行亲核取代反应。由于OH-和RO-具有强碱性,所以醇(ROH)和醚(ROR)本身都不能进行亲核取代反应,它们只有在酸性条件下形成盐
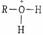 和 和
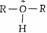 ,使离去基团的碱性相应减弱后(L变为H2O和ROH),才有可能进行亲核取代反应。 ,使离去基团的碱性相应减弱后(L变为H2O和ROH),才有可能进行亲核取代反应。
离去基团的可极化性大小也影响其取代活性。一般说:可极化性越大,其取代活性越强,例如:
I->Br->CI->F-,RS->RO-
这与亲核试剂的活性是一致的。
4.溶剂化效应
溶剂与分子或离子通过静电力而结合的作用叫溶剂化效应。溶剂的性质对共价键的异裂有显著影响,在极性大的溶剂中离子由于溶剂化而被稳定,也可使中性分子离解成为离子。易使R―L离子化的溶剂有利SN1历程,而不利于SN2历程。例如C6H5CH2CI的水解反应,在水中按SN1历程进行,而在丙酮中则按SN2历程进行。溶剂的极性对SN2历程影响比较复杂。
烃基的结构、离去基团的性质、亲核试剂的性能,溶剂的性质等,不仅对亲核取代反应活性、历程方式有影响,而且对亲核取代反应与其副反应(消除反应及重排反应)的竟争也有程度不同影响。
本节共 3 页
1
2 3
下一节 |