|
同羟醛缩合反应一样,都含α-氢的两种不同酯之间的缩合可得四种产物,缺少实用价值。如果其中一个酯不含α-氢,如甲酸酯、苯甲酸酯、草酸酯和碳酸酯等,则可获得比较单一的产物。
甲酸酯活性较高,同含α-氢的酯缩合时,一般醇钠就足以使反应发生。反应结果,α-活泼氢被甲酰基取代,得α-甲酰基酸酯。
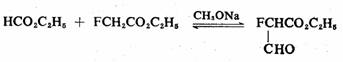
在酯缩合反应中,如果用具有α-氢的酮作亚甲基组分,所得产物为β-二酮。如果酯不含α-氢时,所得β-二酮的产率较高。例如:
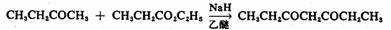
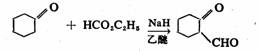
酯缩合反应也可在分子内进行。1,6或1,7位的二元酸酯经缩合,可分别得到五和六元环的β-酮酸酯。该反应又称为狄克曼(Dieckmann)酯缩合反应。例如已二酸二乙酯经此过程可得α-环戊酮甲酸酯。
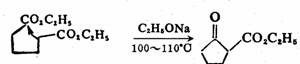
四.克诺文葛尔(Knovenagel)反应
活泼亚甲基化物在氨或胺或其羧酸盐的催化下,与醛、酮的反应称为克诺文葛反应。常用的活泼亚甲基化物包括丙二酸酯、氰乙酸酯和β-酮酸酯等,其α-H的酸性因受两个吸电基团影响,一般较强,使用弱碱如铵盐就可催化反应。关于机理,反应可能是由醛、酮先与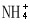 形成亚胺化合物而实现的,后者与碳负离子加成,并经氨的消除而生成α,β-不饱和产物。其过程可能如下: 形成亚胺化合物而实现的,后者与碳负离子加成,并经氨的消除而生成α,β-不饱和产物。其过程可能如下:
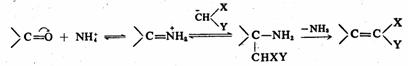
X或Y:CN、CHO、COR(Ar)、COOR、COOH、NO2等。如果缩合反应在吡啶溶液中进行,脱羧一步在反应过程中就可实现,从而生成α,β-不饱和酸衍生物。例如:
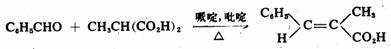
在合成上,克诺文葛尔反应可用于α,β-不饱和酸、腈、硝基化合物等的制备。

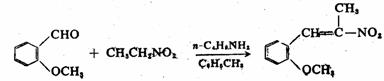
五.柏琴(Perkin)缩合反应
芳醛同脂肪族酸酐在相应羧酸盐催化下缩合,生成β-芳基丙烯酸类化合物的反应称为柏琴缩合反应。反应历程较复杂,在羧酸盐催化下,酸酐形成碳负离子,与芳醛发生亲核加成反应生成一种醇盐。然后发生分子内的酰基转移得β-酰氧基衍生物,经与酸酐作用消除乙酰氧基、水解得产物β-芳基丙烯酸。
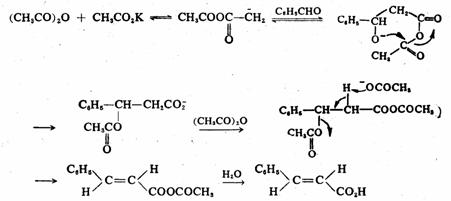
柏琴缩合反应的收率与芳醛上取代基的性质有关。芳环上的吸电子基团促进反应,供电子基团视其位置不同而有不同的影响。例如,芳醛邻位的供电子基(OH、OR)对反应有利,而对位与间位的供电子基团则使反应难于进行。
在合成上,柏琴缩合反应可用于β-芳基丙烯酸的制备。缩合反应一般在较高的温度下进行,这是因为用作活泼亚甲基组分的酸酐的酸性不强,反应所用的碱又是弱碱。因此,缩合反应的产率一般不高。
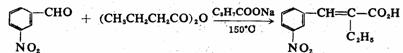
75%
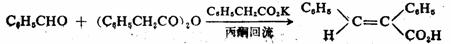
83%
本节共2页
1 2
上一节
下一节
|