|
(3)电环化反应的选择规律
从上可以看出电环化反应的空间过程取决于反应物的HOMO的对称性,若一共轭多烯烃是含有4n个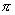 电子的体系,则其热化学反应是顺旋方式进行,光化学是按对旋方式进行;如果共轭多烯烃是含有4n+2个 电子的体系,则其热化学反应是顺旋方式进行,光化学是按对旋方式进行;如果共轭多烯烃是含有4n+2个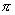 电子的体系,则进行的方式正好与上述相反。这就是伍德华-霍夫曼规则。 电子的体系,则进行的方式正好与上述相反。这就是伍德华-霍夫曼规则。
电环化反应的选择规律
|
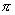 电子数 电子数 |
反应 |
方式 |
|
4n |
热
光 |
顺旋
对旋 |
|
4n+2 |
热
光 |
对旋
顺旋 |
2.解释环加成反应
前线轨道理论认为,象环加成这种涉用到在两个分子之间进行的协同反应,在反应时起决定作用的轨道是一个反应分子的HOMO和另一反应分子的LUMO。当两分子反应时,电子从一个分子的HOMO流进另一分子的LUMO。同时,两个起决定性作用的轨道不仅要有相同的对称性,而且能量必须接近。例如,两分子乙烯进行的[2+2]环加成生成环丁烷的反应。假定两个分子面对面相互接近
,在加热下(即基态时),一分子的HOMO是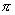 轨道,它对 轨道,它对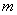 面是对称的,另一分子的LUMO是 面是对称的,另一分子的LUMO是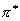 轨道,它对 轨道,它对 轴是对称的,由于两者轨道的对称性不同,因此两分子乙烯在加热下的环加成反应是对称禁阻的。在光的作用下,一个乙烯分子处于激发态,其HOMO为 轴是对称的,由于两者轨道的对称性不同,因此两分子乙烯在加热下的环加成反应是对称禁阻的。在光的作用下,一个乙烯分子处于激发态,其HOMO为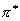 轨道,另一个处于基态乙烯分子的LUMO也是 轨道,另一个处于基态乙烯分子的LUMO也是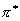 轨道,它们都对 轨道,它们都对 轴对称,所以两分子乙烯可以在光照下进行环加成反应。 轴对称,所以两分子乙烯可以在光照下进行环加成反应。

热反应
对称禁阻
光反应
对称允许
与此相反,在基态时乙烯与1,3-丁二烯的[4+2]加成反应,不论乙烯的HOMO和丁二烯的LUMO(它们都是对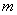 面对称的),还是乙烯的LUMO与丁二烯的HOMO(它们都是对 面对称的),还是乙烯的LUMO与丁二烯的HOMO(它们都是对 轴对称的),都是对称性允许的。因此,乙烯与丁二烯的环加成反应,在加热下都是对称允许的。但其光化学环加成的结果与此相反。 轴对称的),都是对称性允许的。因此,乙烯与丁二烯的环加成反应,在加热下都是对称允许的。但其光化学环加成的结果与此相反。
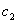 轴对称 轴对称
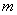 面对称 面对称
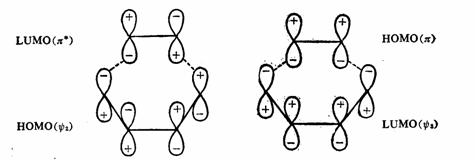
乙烯与丁二烯热化学环加成反应的两种方式
对于1,3-偶极环加成,正如前面提到的,它与[4+2]的D-A反应相似。因此,不论1,3-偶极分子的HOMO和乙烯衍生物的LUMO,还是1,3-偶极分子的LUMO和乙烯衍生物的HOMO,在基态(即在加热下),其轨道的对称性都是允许的。
 面对称 面对称
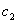 轴对称 轴对称
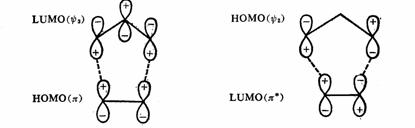
1,3-偶极分子和乙烯衍生物热化学环加成反应的两种方式
通过上述讨论,对于含有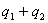 个 个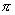 电子的两个反应物的环加成反应,其一般选择规则如下: 电子的两个反应物的环加成反应,其一般选择规则如下:
环加成反应的一般选择规则
|
参加反应的电子数
(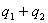 ) ) |
热 |
光 |
|
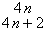
|
禁阻
允许 |
允许
禁阻 |
3.解释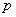 移位反应 移位反应
现以[1,3]氢 移位反应说明如下: 移位反应说明如下:
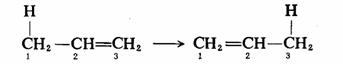
按照前线轨道理论,可以把丙烯按照一个氢原子和一个烯丙基自由基来处理。它们的HOMO分别是氢的1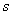 轨道和烯丙基的ψ2轨道。球形对称的氢的1 轨道和烯丙基的ψ2轨道。球形对称的氢的1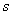 轨道和烯丙基的ψ2轨道另一端成键时,位相应相同,这就需要异面方式才是对称性允许的。但异面移位所要求的几何形状是非常扭歪的,能量很高,因此,在加热下不易进行。 轨道和烯丙基的ψ2轨道另一端成键时,位相应相同,这就需要异面方式才是对称性允许的。但异面移位所要求的几何形状是非常扭歪的,能量很高,因此,在加热下不易进行。
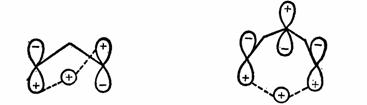
[1,3]氢 移位(异面)
[1,5]氢 移位(异面)
[1,5]氢 移位(同面) 移位(同面)
与此相反,[1,5]氢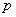 移位同面方式是允许的。它们的HOMO分别为氢的1 移位同面方式是允许的。它们的HOMO分别为氢的1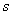 轨道和戊二烯基自由基的ψ3轨道,由于C-1和C-5 轨道和戊二烯基自由基的ψ3轨道,由于C-1和C-5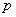 轨道的位相相同,故氢原子能从C-1移位到C-5。 轨道的位相相同,故氢原子能从C-1移位到C-5。
如果移位的基是由 键连接的碳原子,移位的结果可以是构型保持不变,也可以是构型发生转化。例如: 键连接的碳原子,移位的结果可以是构型保持不变,也可以是构型发生转化。例如:
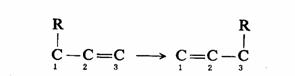
此反应可以看作是由R・和・C―C=C构成的,其中烯丙基自由基的HOMO是ψ2,因此,当R以同面方式进行[1,3]重排时,R的构型必须翻转
。构型保持的例子如:
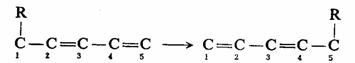
此反应可以看作是由R・和・C―C=C―C=C构成的,后者的HOMO是ψ3,因此,当R以同面方式进行[1,5]重排时,R的构型保持不变,
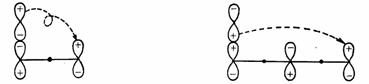
[1,3]碳 移位(构型发生转化)
[1,5]碳 移位(构型发生转化)
[1,5]碳 移位(构型保持) 移位(构型保持)
对于[3,3]碳移位反应,是按照两个烯丙基自由基处理的,其前线轨道是ψ2。若两个烯丙基自由基处于两个接近的平行平面上,则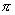 体系两端的 体系两端的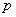 轨道位相都是对称性允许的,可以发生交盖。它是以同面方式进行的同面过程,反应较易进行。 轨道位相都是对称性允许的,可以发生交盖。它是以同面方式进行的同面过程,反应较易进行。
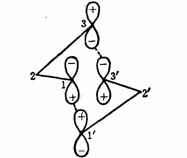
[3,3]碳移位
共 3 页
1
2 3
上一节
下一节 |