|
1,3-丁二烯分子轨道图如下:
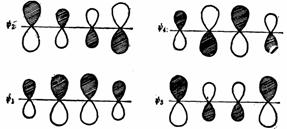
成键轨道
反键轨道
1,3-丁二烯的分子轨道
3.分子轨道的组合和相应能级的简单判断
共轭多烯和环状共轭多烯分子轨道的组合情况及其相应的能级情况,在有机化学中应用十分广泛。应用分子轨道理论,对共轭多烯烃和环状共轭多烯分子轨道的计算和相对稳定性的预测,总结出如下规律。
(1)共轭多烯烃
简单地、定性地判断共轭多烯烃分子轨道的组合情况和相应的能级情况,主要掌握两点:
(a)分子轨道的能量直接与轨道中的节点数相关,最低能级的分子轨道没有节点,有一个节点的为能级较高些的分子轨道,随着节点数增加则分子轨道相应能级依次增高。
(b)每个分子轨道的组合,就任何存在于分子中的对称要素而言,必须是对称的,要么就是反对称的,绝不能是其他,这也是由波函数的对称性质决定的。通常存在于有机分子中的最普遍的对称要素是对称面(m)和对称轴(Cn)。
例如乙烯分子具有一个对称面,垂直于C-Cσ键键轴而且通过此键轴的中点。因此,所有乙烯分子的分子轨道的组合对此平面来说,都必须是对称的或反对称的,不可能是其它。以S(Symmetric)表示对称,A(Asymmetric)表示反对称,分子轨道对m面的对称性如下:
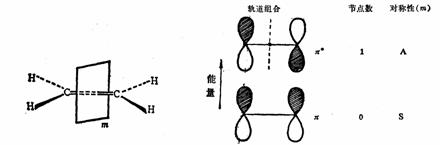
乙烯分子中的对称面(m)
乙烯分子轨道的节点和对称性
1,3-丁二烯分子有一个垂直于π键骨架平面、且通过C2和C3键轴中点的二重对称轴
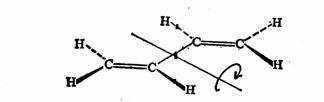
1,3-丁二烯分子中的二重对称轴
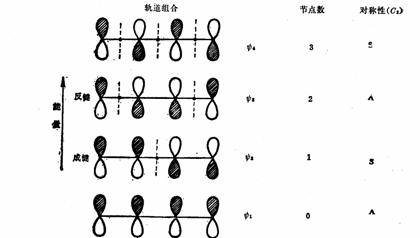
1,3-丁二烯分子中的的节点和对称性

烯丙体系分子轨道组合的节点和对m面的对称性
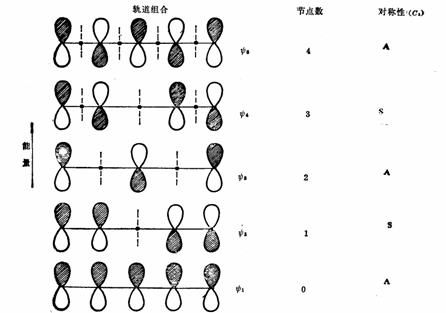
五碳π体系分子轨道组合的节点和对C2轴的对称性
(2)环状共轭多烯
环状共轭多烯分子轨道的排列有如下规律:
偶数 轨道的体系按A类型而奇数轨道的体系按B类型排列:
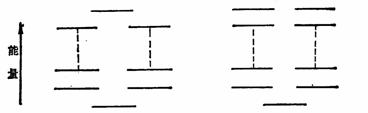
(A)
(B)
不论是偶数还是奇数
轨道的体系,最低能级的轨道只有一个,然后都是成对的、依次升高的简并轨道,偶数体系则还有一个最高能级的单轨道。这样除了最低能级轨道填充两个电子外,偶数体系不考虑最高能级的单轨道,其余电子只有能被4整除时才能充满成键轨道,形成稳定的结构,否则必将在成对的简并轨道中出现孤电子或自旋平行的孤电子对,这就是休克尔提出的4n+2规则的根据。只有P电子数符合4n+2规则(即2,6,10,14,……)的环状共轭
多烯才具有稳定的结构,才具有芳香性,一般称为闭壳层结构。
共
6 页 1
2 3
4 5
6 |