1. 封闭系统的吉布斯函数
对于封闭系统:
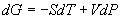
上式给出,物质的量一定时,系统的两个邻近平衡态之间 G 的改变与 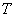 和 P 的改变之间的关系。 和 P 的改变之间的关系。
2. 开放系统的吉布斯函数
对于开放系统,物质的摩尔数要改变,物质摩尔数的改变也会引起 G 的改变。
若以 n 表示摩尔数,则 吉布斯函数的微分可以写成
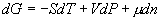
3. 化学势的定义
由 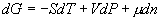 可知 可知
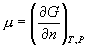 , ,
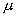 称为化学势。它是温度和压强保持不变的条件下,增加 1 摩尔物质时吉布斯函数的改变。 称为化学势。它是温度和压强保持不变的条件下,增加 1 摩尔物质时吉布斯函数的改变。
由于吉布斯函数是 广延量 ,可令
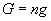 , ,
其中, g 为 一摩尔物质的吉布斯函数
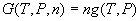
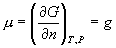
即化学势 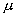 等于摩尔吉布斯函数。 等于摩尔吉布斯函数。
对于开放系统, G 是以 T , P , n 为独立变量的特性函数。
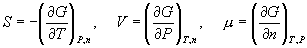 |
![]()